
Más que un Ácido:
El Fascinante Mundo de los Carboxílicos
Introducción:

Los ácidos carboxílicos son compuestos orgánicos que, aunque muchas veces pasan desapercibidos, están presentes en casi todos los aspectos de nuestra vida. Son los héroes silenciosos de la química orgánica: se encuentran en el vinagre con el que aliñamos una ensalada, en el ácido láctico que produce nuestro cuerpo después de hacer ejercicio, e incluso en los aromas y sabores del queso o la mantequilla. Gracias a su estructura química, participan en reacciones esenciales tanto en los seres vivos como en la industria, formando parte de grasas, proteínas, perfumes, medicamentos y muchos productos que usamos a diario. Comprenderlos es descubrir cómo la química da sabor, olor y función a gran parte del mundo que nos rodea.
Antes que nada:
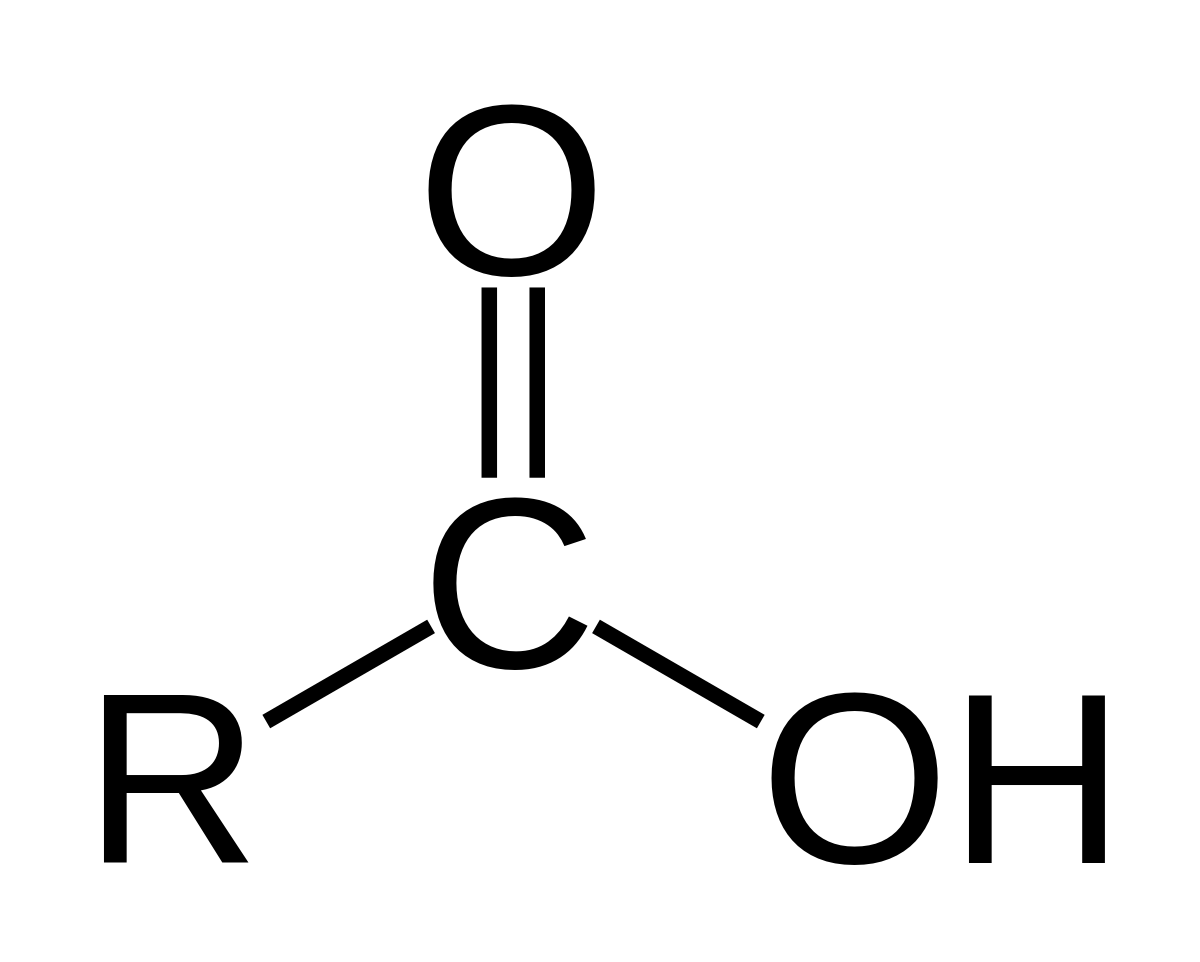
- El grupo carboxilo, es uno de los grupos funcionales más abundantes en química y bioquímica. No sólo los ácidos carboxílicos son importantes en sí mismos, sino el grupo carboxilo es el grupo del cual se deriva una gran familia de compuestos.
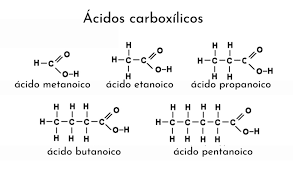
- Es una función de carbono primario. Se caracteriza por tener en el mismo carbono el grupo carbonilo y un oxhidrilo. Se nombran anteponiendo la palabra ácido y con el sufijo oico. Algunos de ellos son más conocidos por sus nombres comunes como el ácido fórmico (metanoico) y ácido acético (etanoico).

Concepto básicos
Que son?
- Los ácidos carboxílicos son compuestos caracterizados por la presencia del grupo carboxilo (-COOH) unido a un grupo alquilo o arilo. Cuando la cadena carbonada presenta un solo grupo carboxilo, los ácidos se llaman monocarboxílicos o ácidos grasos, se les denomina así ya que se obtienen por hidrólisis de las grasas.
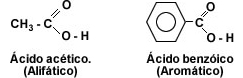
- El primer miembro de la serie alifática de los ácidos carboxílicos es el ácido metanóico o ácido fórmico, este ácido se encuentra en la naturaleza segregado por las hormigas al morder.
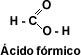
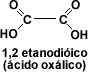
- El primer miembro del grupo aromático es el fenilmetanóico o ácido benzóico. Cuando la cadena carbonada presenta dos grupos carboxilo, los ácidos se llaman dicarboxílicos, siendo el primer miembro de la serie alifática el 1, 2 etanodíoco o ácido oxálico.
Formula
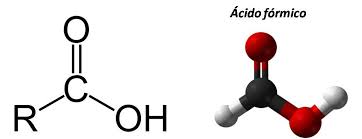
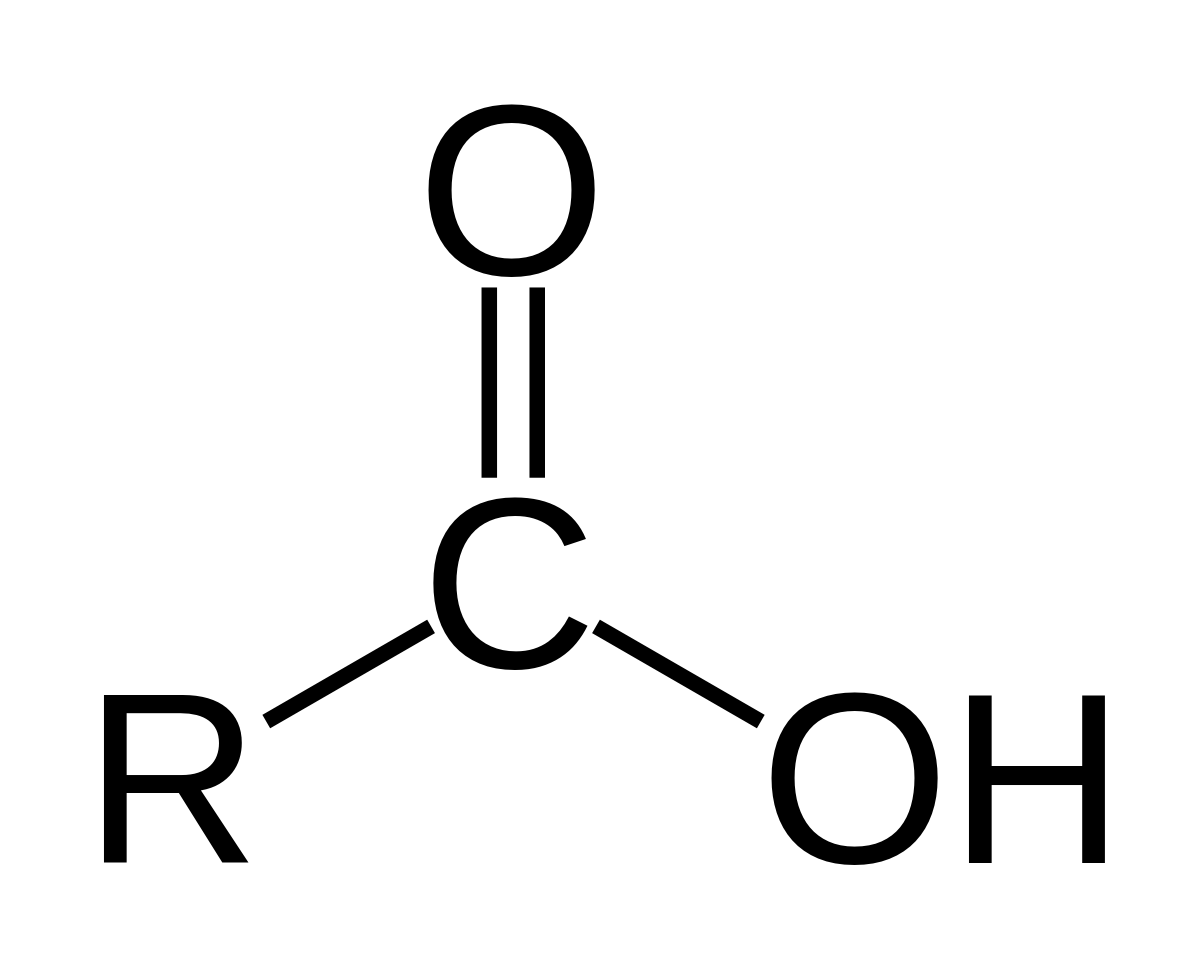
La fórmula general de un ácido carboxílico es R-COOH o R-CO2H, donde R se refiere al grupo alquilo, alquenilo, arilo u otro. Los ácidos carboxílicos se encuentran ampliamente distribuidos en la naturaleza. Ejemplos importantes incluyen los aminoácidos y los ácidos grasos. La desprotonación de un ácido carboxílico da un anión carboxilato. Los ácidos carboxílicos poseen un grupo funcional llamado grupo carboxilo o grupo carboxi
(–COOH). En el grupo funcional carboxilo coinciden sobre el mismo carbono un grupo hidroxilo (-OH) y carbonilo (-C=O).
Nomenclatura
Regla 1. La IUPAC nombra los ácidos carboxílicos reemplazando la terminación -ano del alcano con igual número de carbonos por -oico.
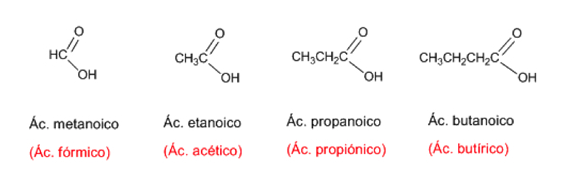
Regla 2. Cuando el ácido tiene sustituyentes, se numera la cadena de mayor longitud dando el localizador más bajo al carbono del grupo ácido. Los ácidos carboxílicos son prioritarios frente a otros grupos, que pasan a nombrarse como sustituyentes.
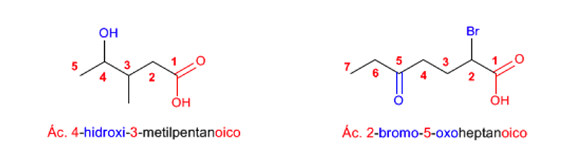
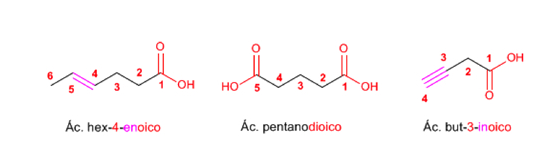
Regla 3. Los ácidos carboxílicos también son prioritarios frente a alquenos y alquinos. Moléculas con dos grupos ácido se nombran con la terminación -dioico.
Regla 4. Cuando el grupo ácido va unido a un anillo, se toma el ciclo como cadena principal y se termina en -carboxílico.


Clasificación:
- Los ácidos carboxílicos generalmente se clasifican según el número de grupos carboxilo (COOH) presentes en la molécula y la naturaleza del grupo alquilo unido al grupo carboxilo.
1. Ácido Monocarboxílico: Estos son ácidos carboxílicos que contienen solo un grupo COOH (carboxilo). Por ejemplo, ácido metanoico (ácido fórmico), ácido etanoico (ácido acético), etc.
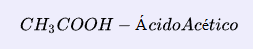
2. Ácido Dicarboxílico: Estos son ácidos carboxílicos que contienen dos grupos COOH (carboxilo). Por ejemplo, ácido etanodioico (ácido oxálico), ácido propanodioico (ácido malónico), etc.
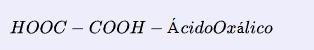
3. Ácido Tricarboxílico: Estos son ácidos carboxílicos que contienen tres grupos COOH (carboxilo). Por ejemplo, 2,2-bis(hidroximetil)propano-1,3-diol (pentaeritritol).
4. Ácido Carboxílico Alifático: Cuando el grupo carboxilo está unido a una cadena alifática, el ácido se llama ácido carboxílico alifático. Por ejemplo, ácido propanoico.
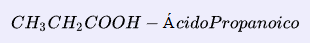
5. Ácido Carboxílico Aromático: Cuando el grupo carboxilo está unido a un anillo aromático, el ácido se llama ácido carboxílico aromático. Por ejemplo, ácido benzoico.
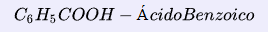

Propiedades físicas
1. Solubilidad: El grupo carboxilo –COOH confiere carácter polar a los ácidos y permite la formación de puentes de hidrógeno entre la molécula de ácido carboxílico y la molécula de agua. La presencia de dos átomos de oxígeno en el grupo carboxilo hace posible que dos moléculas de ácido se unan entre sí por puente de hidrógeno doble, formando un dímero cíclico.
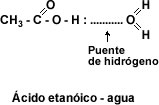
- Esto hace que los primeros cuatro ácidos monocarboxílicos alifáticos sean líquidos completamente solubles en agua. La solubilidad disminuye a medida que aumenta el número de átomos de carbono. A partir del ácido dodecanóico o ácido láurico los ácidos carboxílicos son sólidos blandos insolubles en agua.
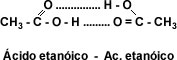
- Los ácidos carboxílicos son solubles en solventes menos polares, tales como éter, alcohol, benceno, etc. Los ácidos carboxílicos hierven a temperaturas aún más altas que los alcoholes. Estos puntos de ebullición tan elevados se deben a que un par de moléculas del ácido carboxílico se mantienen unidas no por un puente de hidrógeno sino por dos
2. Punto de ebullición: Los ácidos carboxílicos presentan puntos de ebullición elevados debido a la presencia de doble puente de hidrógeno.

3. Punto de fusión: El punto de fusión varía según el número de carbonos, siendo más elevado el de los ácidos fórmico y acético, al compararlos con los ácidos propiónico, butírico y valérico de 3, 4 y 5 carbonos, respectivamente. Después de 6 carbonos el punto de fusión se eleva de manera irregular.
- Esto se debe a que el aumento del número de átomos de carbono interfiere en la asociación entre las moléculas. Los ácidos monocarboxílicos aromáticos son sólidos cristalinos con puntos de fusión altos respecto a los ácidos alifáticos..
- Los ácidos fórmico y acético (1, 2 carbonos) son líquidos de olores irritantes. Los ácidos butíricos, valeriano y capróico (4, 5 y 6 carbonos) presentan olores desagradables. Los ácidos con mayor cantidad de carbonos presentan poco olor.

- Las sales de los ácidos carboxílicos son sólidos cristalinos formados por iones positivos y negativos, unidos por fuertes fuerzas electrostáticas que solo pueden romperse con altas temperaturas o solventes muy polares. Al calentarse demasiado (300–400 °C), suelen descomponerse antes de fundirse. Se forman cuando una base fuerte desprotona completamente a un ácido carboxílico, originando un ión carboxilato y un catión, cuya combinación da lugar a la sal correspondiente.

Propiedades Quimicas
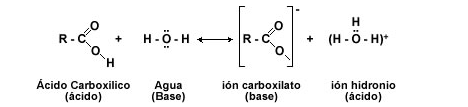
- El comportamiento químico de los ácidos carboxílicos está determinado por el grupo carboxilo -COOH. Esta función consta de un grupo carbonilo (C=O) y de un hidroxilo (-OH). Donde el -OH es el que sufre casi todas las reacciones: pérdida de protón (H+) o reemplazo del grupo –OH por otro grupo.
- Formación de hidrólisis de nitrilos. Los mejores reactivos para convertir los ácidos carboxílicos en cloruros de ácido son el cloruro de tionilo (SOCl2) y el cloruro de oxalilo (COCl)2, porque forman subproductos gaseosos que no contaminan al producto. El cloruro de oxalilo es muy fácil de emplear porque hierve a 62ºC y se evapora de la mezcla de reacción.
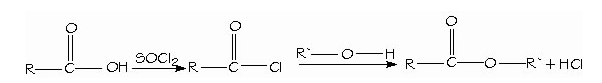
- Síntesis y empleo de cloruros de ácido. Los ácidos carboxílicos se convierten directamente en ésteres mediante la esterificación de Fischer, al reaccionar con un alcohol con catálisis ácida.
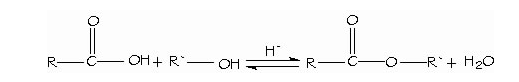
- Condensación de los ácidos con los alcoholes. Esterificación de Fischer. El hidruro de litio y aluminio (LiAlH4) reduce los ácidos carboxílicos para formar alcoholes primarios. El aldehído es un intermediario en esta reacción, pero no se puede aislar porque se reduce con mayor facilidad que el ácido original.
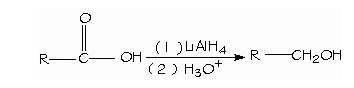
- Reducción de los ácidos carboxílicos. Un método general para preparar cetonas es la reacción de un ácido carboxílico con 2 equivalentes de un reactivo de organolitio.
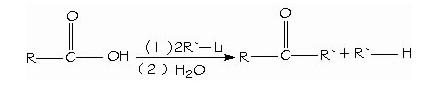
Usos
Los ácidos carboxílicos son ampliamente utilizados en diversas industrias. Algunos de sus usos incluyen:
- Industria Alimentaria: Ciertos ácidos carboxílicos, especialmente los de cadena corta, se utilizan como aditivos alimentarios y a menudo se emplean en la preparación de vinagre (ácido etanoico).
- Farmacéuticos: Muchos ácidos carboxílicos se utilizan en la fabricación de productos farmacéuticos. La aspirina, un analgésico de uso común, es ácido acetilsalicílico. Otro ejemplo es la penicilina, un antibiótico que también tiene un grupo funcional de ácido carboxílico.
3. Textiles y Colorantes: Los ácidos carboxílicos se usan en la producción de colorantes y textiles. Por ejemplo, el ácido acético se emplea en la producción de ácido tereftálico, que luego se utiliza para fabricar fibras de poliéster y botellas de plástico.
4. Alimentos para Animales: Ácidos carboxílicos como el ácido fórmico y el ácido propiónico se utilizan como conservantes en los alimentos para animales. Ayudan a prevenir el crecimiento de bacterias y hongos perjudiciales.
5. Caucho: Los ácidos carboxílicos también se utilizan en la industria del caucho para el proceso de vulcanización, lo que ayuda a hacer el caucho más duradero.
Grupo funcional:
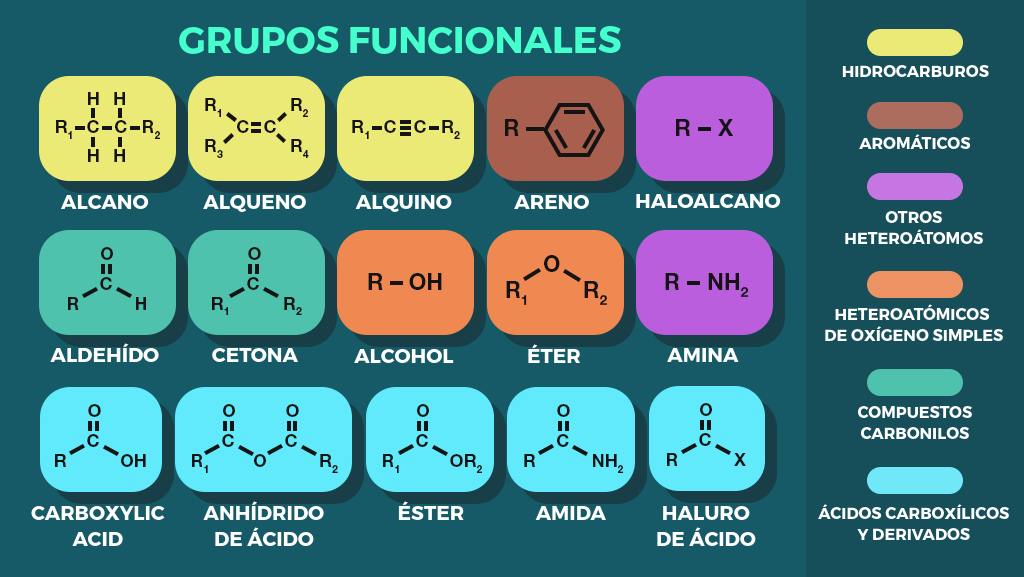
Otros:
Ejemplos:
- Ácido fórmico: (HCOOHcap H cap C cap O cap O cap H𝐻𝐶𝑂𝑂𝐻): También conocido como ácido metanoico.
- Ácido acético: (CH3COOHcap C cap H sub 3 cap C cap O cap O cap H𝐶𝐻3𝐶𝑂𝑂𝐻): El componente principal del vinagre.
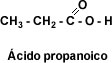
- Ácido propiónico: (CH3CH2COOHcap C cap H sub 3 cap C cap H sub 2 cap C cap O cap O cap H𝐶𝐻3𝐶𝐻2𝐶𝑂𝑂𝐻): También llamado ácido propanoico.
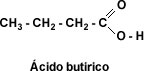
- Ácido butírico: (CH3(CH2)2COOHcap C cap H sub 3 open paren cap C cap H sub 2 close paren sub 2 cap C cap O cap O cap H𝐶𝐻3(𝐶𝐻2)2𝐶𝑂𝑂𝐻): Encontrado en la mantequilla rancia.
Datos curiosos
- Transporte de oxígeno: Aunque no son los ácidos en sí, la química relacionada con el transporte de oxígeno en la sangre involucra la liberación de dióxido de carbono (una especie de ácido carbónico) en los pulmones para poder inhalar aire nuevo.
- Metabolismo: Son esenciales en el metabolismo, como el piruvato carboxilasa, que mantiene el equilibrio de los metabolitos en el ciclo del ácido tricarboxílico.
- Inflamación: Bloquean las enzimas que producen prostaglandinas, lo que ayuda a reducir la inflamación y el dolor. Esto es lo que hace que la aspirina sea un analgésico y un antiinflamatorio.
- Naturaleza y vida diaria: Están presentes en frutas, aceites, leche, sudor y hasta en perfumes. Por ejemplo, los ácidos grasos que forman parte de los aceites vegetales también son carboxílicos, lo que los hace esenciales para la vida y la industria.
- Ácidos que curan: Algunos ácidos carboxílicos se usan en medicamentos o tratamientos dermatológicos. El ácido salicílico, por ejemplo, proviene originalmente de la corteza del sauce y es la base para fabricar la aspirina.
- Su versatilidad química: Son de los compuestos más útiles en la química orgánica porque pueden transformarse en otros grupos funcionales: ésteres, amidas, anhídridos y alcoholes. Esto los convierte en piezas clave para crear nuevos materiales y productos.
- El ácido más simple, pero poderoso: El ácido fórmico (HCOOH), el más pequeño de todos, fue aislado por primera vez de hormigas rojas (de ahí su nombre). A pesar de su tamaño, tiene una gran capacidad corrosiva y energética.
Conclusión
Los ácidos carboxílicos son compuestos muy importantes en la vida diaria y en la industria. Están presentes en alimentos, medicamentos y productos de limpieza, mostrando su gran utilidad. Conocerlos permite entender mejor cómo la química influye en nuestro entorno y en la creación de sustancias esenciales para el bienestar humano.